Curiosidades
Nesta seção você terá acesso a inúmeras curiosidades do nosso cotidiano, todas relacionadas com a Química Experimental, saber como são produzidos os mais variados objetos e de quê eles são feitos. Confira!
A Química do Amor
Cupido usando o arco e a flecha impregnados de noradrenalina.
O sentimento não afeta só o nosso ego de forma figurada, mas está presente de forma mais concreta, produz reações visíveis em nosso corpo inteiro. Se não fosse assim como explicar as mãos suando, coração acelerado, respiração pesada, olhar perdido (tipo "peixe morto"), o ficar rubro quando se está perto do ser amado?
Afinal, o amor tem algo a ver com a Química? Na verdade O AMOR É QUÍMICA! Todos os sintomas relatados acima têm uma explicação científica: são causados por um fluxo de substâncias químicas fabricadas no corpo da pessoa apaixonada. Entre essas substâncias estão: adrenalina, noradrenalina, feniletilamina, dopamina, oxitocina, a serotonina e as endorfinas. Viu como são necessários vários hormônios para sentir aquela sensação maravilhosa quando se está amando?
A dopamina produz a sensação de felicidade, a adrenalina causa a aceleração do coração e a excitação. A noradrenalina é o hormônio responsável pelo desejo sexual entre um casal, nesse estágio é que se diz que existe uma verdadeira química, pois os corpos se misturam como elementos em uma reação química.
Mas acontece que essa sensação pode não durar muito tempo, neste ponto os casais têm a impressão que o amor esfriou. Com o passar do tempo o organismo vai se acostumando e adquirindo resistência, passa a necessitar de doses cada vez maiores de substâncias químicas para provocar as mesmas sensações do início. É aí que entra os hormônios ocitocina e vasopressina, são eles os responsáveis pela atração que evolui para uma relação calma, duradoura e segura, afinal, o amor é eterno!
Aço inoxidável

Existem alguns aços que são resistentes à corrosão, são os inoxidáveis. Esses aços são caracterizados pela resistência à corrosão atmosférica, pois quando estão ligados com outros metais como o Cromo e o Níquel, ficam menos reativos. São fabricados a partir do ferro-gusa em altos-fornos.
A expressão aço inoxidável nos dá uma idéia de um material que não se destrói mesmo quando submetido aos mais violentos abusos, mas na verdade esse tipo de aço não é eterno, só apresenta uma maior resistência à corrosão quando submetido a um determinado meio ou agente agressivo.
A resistência à oxidação e corrosão do aço inoxidável se deve principalmente à presença do cromo, que permite a formação de uma película finíssima de óxido de cromo sobre a superfície do aço, que é impermeável e insolúvel nos meios corrosivos usuais.
Assim, podemos definir como aço inoxidável o grupo de ligas ferrosas resistentes à oxidação e corrosão, que contenham no mínimo 12% de cromo.
O aço é facilmente corrosível por ação química ou eletroquímica. O próprio meio ambiente o danifica: o oxigênio do ar, por exemplo, quando entra em contato com o ferro contido no aço forma o óxido de ferro causando alterações naturais, porém, indesejáveis. O próprio nome já indica, aço inoxidável é um aço de alta-liga resistente à ação deteriorante do oxigênio, ou seja, não sofre oxidação. Apresenta propriedades físico-químicas superiores aos aços comuns, sendo a alta resistência à oxidação atmosférica a sua principal característica.
Principais utilizações dos aços inoxidáveis:
• Utensílios domésticos: Grandes eletrodomésticos e pequenos utensílios, como garfos, faca e talheres em geral, e também panelas.
• Em automóveis: produção de peças para veículos automotores como, por exemplo, canos de descarga.
• Na construção civil: em edifícios e casas;
• Na Indústria: alimentação, produtos químicos e petróleo.
Calor no processo de secar roupas
.jpg)
Como é possível que as roupas sequem no varal, se elas não estão quentes o suficiente para fazer com que a água aprisionada a elas ferva e evapore?
Até onde sabemos, o processo de evaporação se dá a altas temperaturas (acima de 100°C), ou seja, para o líquido chegar ao estado de vapor precisa estar superaquecido.
Ao lavar suas roupas, você permite que moléculas de água fiquem aderidas ao tecido. Portanto, a água não está livre no ambiente, ela se encontra alojada em meio à roupa. Por mais que você conceda fontes de aquecimento, como a secagem ao sol, por exemplo, a água ainda está lá, bem escondidinha. A menos que ela resolva se expor na superfície da roupa. O calor neste caso pode ser definido como a energia que as moléculas possuem, quanto maior o calor, maior será a energia para as moléculas escaparem para fora do tecido.
A uma temperatura de 20°C, algumas moléculas terão energia suficiente para se deslocarem completamente da roupa para o ar. A certo momento, todas as moléculas já terão escapado e evaporado em razão do contato com o ambiente quente, é o instante em que identificamos a roupa como seca.
Em algumas épocas do ano, no período de seca (estiagem), o processo de secar roupas é acelerado. A baixa umidade relativa do ar faz com que este roube a água contida na roupa. Desta forma, é comum a prática de se colocar toalhas úmidas na cabeceira de camas para facilitar a respiração na hora de dormir, uma vez que a atmosfera próxima irá ficar umidificada.
Ácido araquidônico na gravidez

Mulheres grávidas se preocupam com a saúde de seus bebês e costumam obedecer à risca a dieta alimentar indicada pelos médicos. O que nem todas sabem é sobre a composição de alimentos, como o leite materno, por exemplo, e por que ele é tão essencial para a vida de seu filho.
Dentre as substâncias presentes no leite temos algumas pouco conhecidas, como o ácido araquidônico, que é fundamental para o desenvolvimento de fetos e bebês. Vejamos o porquê.
Uma mulher grávida já fornece esse ácido através da placenta, e após o bebê nascer ela continua a fornecê-lo através do leite. A importância dessa parceria pode ser comprovada quando acontece o nascimento prematuro (antes de completar 9 meses), o inconveniente impede que a mãe transfira o ácido a seu filho até o período completo de gestação. E o quadro pode se agravar se a criança prematura não for alimentada com leite materno.
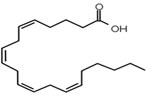
Estrutura química do ácido araquidônico
A falta de ácido araquidônico é denotada em bebês prematuros através de problemas visuais, incapacidades físicas (paralisia mental, dificuldades para ficar em pé) e retardo do crescimento (bebês menores).
Como agem os xampus e condicionadores em seu cabelo

Ambos possuem, em sua formulação, moléculas de surfactantes. Os xampus e condicionadores diferem, basicamente, na carga do surfactante: os xampus contém surfactantes aniônicos, enquanto que os condicionadores têm surfactantes catiônicos. Quando o cabelo está sujo, ele contém óleo em excesso e uma série de partículas de poeira e outras sujeiras que aderem à superfície do cabelo. Esta mistura é, geralmente, insolúvel em água - daí a necessidade de um xampu para o banho. O surfactante ajuda a solubilizar as sujeiras, e lava o cabelo.
Um problema surge do fato de que surfactantes aniônicos formam complexos estáveis com polímeros neutros ou proteínas, como é o caso da queratina. O cabelo, após o uso do xampu, fica carregado eletrostaticamente, devido a repulsão entre as moléculas de surfactantes (negativas) "ligadas" à queratina. É aí que entra o condicionador: os surfactantes catiônicos interagem fracamente com polímeros e proteínas neutras, e são capazes de se agregar e arrastar as moléculas de xampu que ainda estão no cabelo. Nos frascos de condicionadores existem, ainda, alguns produtos oleosos, para repor a oleosidade ao cabelo, que foi extraída com o xampu.
O cabelo, após o condicionador, fica menos carregado e, ainda, com mais oleosidade.
Segundo este critério, não existe xampu "2 em 1", ou seja, uma formulação capaz de conter tanto um surfactante aniônico como um catiônico. Os produtos encontrados no mercado que se dizem ser "xampu 2 em 1" são, na verdade, xampus com surfactantes neutros ou, ainda, surfactantes aniônicos com compostos oleosos, que minimizam o efeito eletrostático criado pelo xampu normal.
Fonte:
https://www.cienciaquimica.hpg.com.br/curiosidades/curiosidades.htm#Ambos